- 電池って、中にどうやって電気が入っているの?
- 乾電池はなぜ使い切ると「空」になるの?
- スマホのリチウムイオン電池はなぜ充電できるの?
- 電池を直列につなぐと電圧が上がるのはなぜ?
- 電池の正体は「化学反応で電気を生み出す装置」であること
- 乾電池が電気を出す仕組みを「酸化還元反応」でスッキリ理解
- リチウムイオン電池が充電・放電できる仕組み
- 電池の直列つなぎ・並列つなぎで「何が変わるのか」
リモコン、懐中電灯、スマホ、ワイヤレスイヤホン、電気自動車——。私たちの生活は、「電池」なしには成り立ちません。
でも、考えてみると不思議ですよね。コンセントにつないでいないのに電気が出てくる。あの小さな筒の中に、一体何が入っているのでしょうか?
「電気が詰まっている」と思っている方も多いかもしれませんが、実は違います。
電池の中に「電気」は入っていません。入っているのは「化学物質」です。
電池とは、化学物質が反応するときに発生するエネルギーを、電気エネルギーとして取り出す装置です。言い換えれば、電池は「化学エネルギーを電気エネルギーに変換するマシン」なのです。
この記事では、乾電池からスマホのリチウムイオン電池まで、電池が電気を出せる「本当の理由」をやさしく解説します。化学の知識は不要です。たとえ話と図で理解できるようにしていますので、安心して読み進めてください。
目次
🔋 そもそも電池とは何か?|「化学反応で電子を押し出すポンプ」
電池の中に「電気」は入っていない
多くの人が「電池 = 電気が入っている容器」とイメージしがちですが、これは誤解です。
電池の中に入っているのは「化学物質」——つまり、特定の金属や液体(電解液)です。これらの化学物質が反応することで、電子(電気の正体)が移動し、電流が流れるのです。
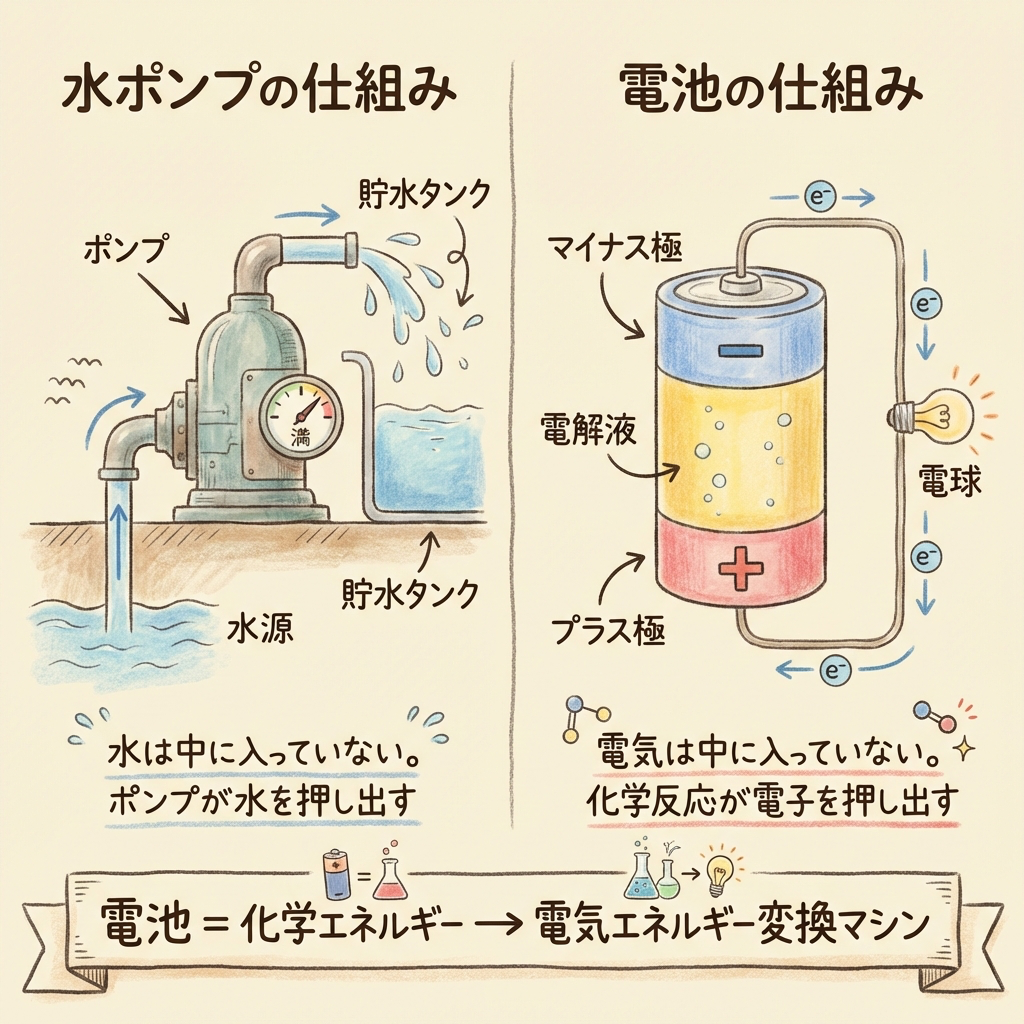
わかりやすく言えば、電池は「化学反応という燃料を使って、電子を押し出すポンプ」のようなものです。
水のポンプ
ポンプの中に
「水は入っていない」
ポンプが動くことで
水を押し出す力(水圧)を生む
燃料が切れたら止まる
電池
電池の中に
「電気は入っていない」
化学反応で
電子を押し出す力(電圧)を生む
化学物質が尽きたら切れる
電池の3つの部品|プラス極・マイナス極・電解液
すべての電池は、基本的に3つの部品で構成されています。
| 部品 | 別名 | 役割 |
|---|---|---|
| ➖ マイナス極 | 負極 | 電子を放出する側。化学反応で電子を「手放す」物質でできている |
| ➕ プラス極 | 正極 | 電子を受け取る側。化学反応で電子を「受け入れる」物質でできている |
| 💧 電解液 | 電解質 | プラス極とマイナス極の間をイオンが移動する通路。電池の内部で化学反応を仲介する |
マイナス極で電子が「生まれ」、導線(外部回路)を通ってプラス極に「到着」する。この電子の流れが電流です。電池の内部では、電解液を通じてイオンが移動することで回路が完成します。
電池は「電子を生む工場(マイナス極)」と「電子を受け取る倉庫(プラス極)」と「内部の通路(電解液)」の3点セットです。外側の導線が電子の通り道、内側の電解液がイオンの通り道。この「外ルート+内ルート」で、電気の回路がぐるっと一周つながるのです。
🔦 乾電池の仕組み|「2種類の金属」が電子を押し出す
電池の発明は「カエルの足がピクッと動いた」ことから始まった
電池の歴史は、18世紀のイタリアにさかのぼります。
解剖学者のガルバーニがカエルの足に2種類の金属を当てたところ、足がピクッと動きました。これを「動物電気」と考えたガルバーニに対して、物理学者のボルタは「金属の組み合わせが電気を生んでいる」と反論。そして1800年、亜鉛と銅の板を食塩水に浸した紙で挟んで積み重ねた「ボルタの電堆(でんたい)」——世界初の電池を発明しました。
電圧の単位「ボルト(V)」は、このボルタの名前に由来しています。
乾電池の中身|亜鉛・二酸化マンガン・電解液
現在もっとも身近な乾電池(アルカリ乾電池)の中身を見てみましょう。
| 部品 | 素材 | 役割 |
|---|---|---|
| ➖ マイナス極 | 亜鉛(Zn) | 化学反応で電子を手放す(酸化される) |
| ➕ プラス極 | 二酸化マンガン(MnO₂) | 電子を受け取る(還元される) |
| 💧 電解液 | 水酸化カリウム水溶液 | イオンの通り道 |
電気が生まれる仕組み|「電子を手放したがる金属」と「電子が欲しい物質」
ここが一番大事なポイントです。難しい化学式は使いませんので、たとえ話で理解しましょう。
学校で、お菓子を大量に持っている子(亜鉛)と、お菓子が足りなくて欲しがっている子(二酸化マンガン)がいるとします。
亜鉛(マイナス極)が電子を手放す
亜鉛は「電子を手放しやすい」性質を持つ金属です。化学反応が起きると、亜鉛原子は電子を2個放出します。これを「酸化」と呼びます。(お菓子を差し出す子)
放出された電子が導線を通って移動する
手放された電子は、電池の外側の導線を通ってプラス極に向かいます。この電子の流れが「電流」です。(お菓子が廊下を通って隣の教室へ運ばれる)
二酸化マンガン(プラス極)が電子を受け取る
プラス極に到着した電子は、二酸化マンガンに受け取られます。これを「還元」と呼びます。(お菓子を受け取った子が満足する)
この「電子を手放す(酸化)」と「電子を受け取る(還元)」がセットで起きる反応を、「酸化還元反応」と呼びます。電池の電気は、この酸化還元反応から生まれているのです。
マイナス極の物質が「電子を手放したがる力」と、プラス極の物質が「電子を欲しがる力」の差が、電池の電圧(起電力)になります。
アルカリ乾電池の場合、亜鉛と二酸化マンガンの「電子の押し付け合い」の差が約1.5V。だから乾電池1本は1.5Vなのです。
「電流はプラスからマイナスに流れる」と習いますが、実際に動いている電子はマイナスからプラスに移動しています。電流の向きは歴史的な約束事で、電子の流れと逆方向に定義されています。少しややこしいですが、電験三種でも出題されるポイントです。

⚡ なぜ電池は「空」になる?|一次電池と二次電池の違い
乾電池が空になる理由|化学物質が「使い切られる」から
乾電池を使い続けると、いつか電気が出なくなりますよね。これは、マイナス極の亜鉛が化学反応ですべて別の物質に変わってしまうからです。
たとえるなら、ろうそくと同じです。ろうそくはロウ(燃料)を燃やして光を出しますが、ロウがなくなれば火は消えます。乾電池も、亜鉛という「化学的な燃料」が反応し尽くしたら、もう電子を出す力がなくなるのです。
一次電池
(使い切りタイプ)
化学反応が一方通行
反応した物質は
元に戻せない
使い切ったら捨てる
例:アルカリ乾電池
マンガン乾電池
二次電池
(充電タイプ)
化学反応を逆回しにできる
外から電気を流すと
物質が元に戻る
何度も繰り返し使える
例:リチウムイオン電池
ニッケル水素電池
・一次電池 = 化学反応が一方通行。使い切ったら終わり(ろうそく)
・二次電池 = 化学反応を逆回しにできる。充電すれば復活する(充電式のろうそく…?)
「充電」とは、外から電気を流すことで、反応済みの物質を元の状態に戻すことです。
📱 リチウムイオン電池の仕組み|「リチウムイオンの引っ越し」で充放電する
スマホの電池はどう動いている?
スマホ、ノートPC、電気自動車に使われているリチウムイオン電池は、世界で最も広く使われている二次電池です。2019年には、開発に貢献した吉野彰氏がノーベル化学賞を受賞しました。
リチウムイオン電池の仕組みを一言で言うと、「リチウムイオン(Li⁺)がプラス極とマイナス極の間を行ったり来たりする」ことで充電と放電を繰り返します。
🔋 放電時(スマホを使っているとき)
(黒鉛)
(コバルト酸
リチウム等)
リチウムイオンがマイナス極→プラス極に引っ越し。
同時に電子が外部回路を通ってプラス極へ → これが電流
🔌 充電時(スマホを充電しているとき)
充電器から電気を流すと、リチウムイオンが逆方向に引っ越し。
化学反応が巻き戻り、エネルギーが再充填される
リチウムイオン電池の名前は、この「リチウムイオンが行き来する」仕組みに由来しています。引っ越しのたとえで言えば、放電はリチウムイオンが「マイナス極の家からプラス極の家に引っ越す」こと。充電は「プラス極の家から元のマイナス極の家に帰る」ことです。
充電・放電を繰り返すと、電極の材料が少しずつ劣化し、リチウムイオンが移動しにくくなります。これがスマホの「バッテリーのヘタリ」です。一般的に約500〜1,000回の充放電で容量が70〜80%程度に低下すると言われています。

🔗 電池の直列つなぎ・並列つなぎ|電圧と容量はどう変わる?
直列つなぎ|電圧が「足し算」になる
懐中電灯に乾電池を2本入れるとき、プラス極とマイナス極が交互になるように入れますよね。これが直列つなぎです。
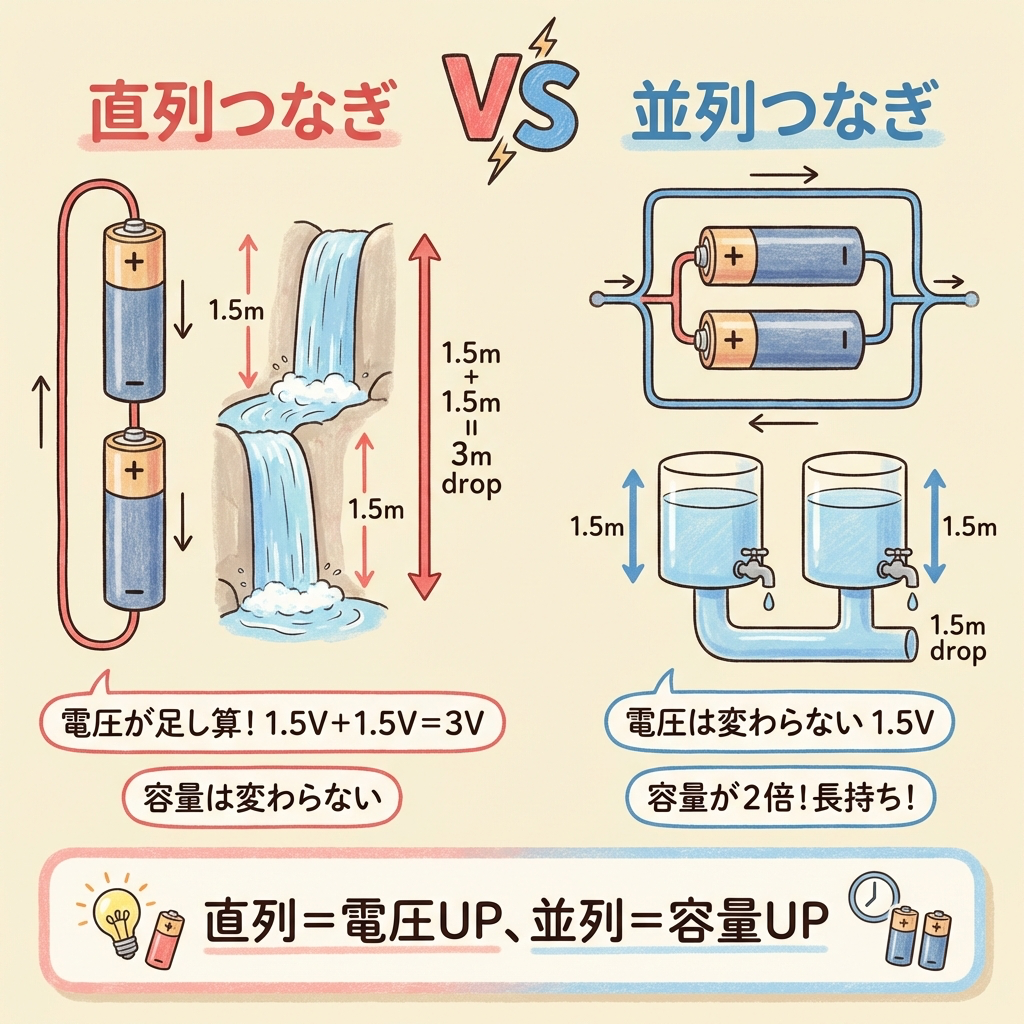
直列につなぐと、電圧が足し算になります。1.5Vの乾電池を2本直列にすれば3V、3本なら4.5Vです。
たとえるなら、滝を重ねるようなものです。1段の滝の落差が1.5mなら、2段重ねれば落差3m。落差が大きいほど水の勢い(電圧)は上がりますが、流れる水の量(電流を流せる時間 = 容量)は変わりません。
並列つなぎ|容量(持ち時間)が増える
並列つなぎは、プラス極同士、マイナス極同士を接続する方法です。
並列につないでも電圧は変わりません(1.5V + 1.5V = 1.5V)。その代わり、容量(電気を供給できる時間)が2倍になります。
たとえるなら、水の貯水タンクを2つ並べるようなものです。タンク1つの水位(電圧)は変わりませんが、使える水の総量(容量)は2倍になります。
| 比較項目 | 🔗 直列つなぎ | 🔗 並列つなぎ |
|---|---|---|
| つなぎ方 | +と−を交互に接続 | +同士、−同士を接続 |
| 電圧 | 足し算になる 1.5V × 2 = 3V |
変わらない 1.5Vのまま |
| 容量(持ち時間) | 変わらない | 足し算になる (2倍長持ち) |
| たとえ | 滝を重ねる (落差が上がる) |
貯水タンクを並べる (水量が増える) |
| 用途 | 高い電圧が必要な機器 (懐中電灯、リモコン) |
長時間使いたいとき (大容量バッテリー) |
電験三種の理論科目では、電池の内部抵抗を考慮した回路計算が出題されます。理想的な電池は電圧だけを持ちますが、現実の電池は内部に「小さな抵抗」を持っています。この内部抵抗を含む回路はキルヒホッフの法則で解く必要があります。
📋 電池の種類と特徴を一覧で整理
【保存版】身近な電池の比較表
| 電池の種類 | 分類 | 電圧 | 主な用途 | 特徴 |
|---|---|---|---|---|
| マンガン乾電池 | 一次 | 1.5V | リモコン、時計 | 安い。小電流向き。休ませると回復する |
| アルカリ乾電池 | 一次 | 1.5V | 懐中電灯、おもちゃ | マンガンの上位互換。大電流OK |
| ニッケル水素 電池 |
二次 | 1.2V | 充電式の単3・単4 | 乾電池の代わりに使える充電池 |
| リチウムイオン 電池 |
二次 | 3.7V | スマホ、ノートPC、EV | 軽い・高電圧・大容量。現代の主役 |
| 鉛蓄電池 | 二次 | 2.0V (セル) |
自動車バッテリー、UPS | 安い・大電流OK。重いのが弱点 |
電験三種では鉛蓄電池が頻出です。自動車のバッテリーに使われており、正極に二酸化鉛(PbO₂)、負極に鉛(Pb)、電解液に希硫酸(H₂SO₄)を使用します。また、電力科目では蓄電池を用いた電力系統の安定化や、非常用電源としてのUPS(無停電電源装置)が問われることもあります。

📝 まとめ|電池が電気を出せる理由はたった1つ
- 電池の中に「電気」は入っていない。入っているのは化学物質
- 電池 = 化学エネルギーを電気エネルギーに変換する装置
- マイナス極が電子を「手放し(酸化)」、プラス極が電子を「受け取る(還元)」。この酸化還元反応で電子が移動し、電流が流れる
- 電池の電圧 = マイナス極の「電子を手放す力」とプラス極の「電子を欲しがる力」の差
- 一次電池(乾電池):化学反応が一方通行。使い切ったら終わり
- 二次電池(リチウムイオン電池等):化学反応を逆回しにできる。充電で復活
- リチウムイオン電池は「リチウムイオンの引っ越し」で充放電する
- 直列つなぎ:電圧が足し算。並列つなぎ:容量が足し算
電池が電気を出せる理由を一言でまとめると——
電子を手放したがる物質と、電子が欲しい物質を組み合わせて、電子が「外の導線」を通って移動するように仕向ける。この巧みな設計が、電池という発明の核心です。
そしてこの「電子の流れ」を制御し、計算し、活用するのが電気工学の世界です。電池の仕組みを理解できた今、あなたは電気を学ぶための最初の一歩をすでに踏み出しています。
リモコンの電池を交換する何気ない瞬間にも、亜鉛と二酸化マンガンの酸化還元反応という壮大なドラマが起きていました。スマホを充電するたびに、リチウムイオンが極間を行き来しています。日常の「当たり前」を科学の目で見ると、世界がちょっと違って見えるかもしれません。
📚 次に読むべき記事
電池から飛び出す「電子」の正体を深堀り。電流・電圧・エネルギーの関係がスッキリわかります。
電池の「1.5V」「3.7V」って何の数字?電圧・電流・電力の単位を身近なたとえで解説。
電池が電気を流すには「回路」が必要。なぜ一周つながっていないと電流が流れないのかを解説。
電池の電圧と回路の抵抗から電流を計算する「オームの法則」。電気計算の第一歩。
電池の直列・並列を学んだら、抵抗の直列・並列もマスター。回路計算の基礎が固まります。
内部抵抗を持つ電池を含む回路の計算に必須。キルヒホッフの法則は電験三種の超頻出テーマです。
電験三種の理論科目を始めるなら、まずここから。電圧・電流・抵抗を水のたとえで完全理解。
電池の電圧=電位差。この「電位差」がなぜ電流を流す原動力なのかをさらに深く理解。
電池の電極にはなぜ金属が使われるのか。導体・絶縁体・半導体の違いを図解で学べます。
電気の学習を本格的に始めるなら、効率的な学習環境づくりから。合格者おすすめのアイテム。
電気に興味が出てきたら、電験三種の全体像を把握。学習計画の立て方がわかります。


