- 「鉛蓄電池の電解液は希硫酸?水酸化カリウム?」と聞かれて固まった
- NAS電池とリチウムイオン電池の違いが曖昧で、正誤問題を「なんとなく」で選んでいる
- 燃料電池は「水素と酸素で発電する」くらいしか知らない
- 一次電池・二次電池・燃料電池の根本的な違い
- 電験三種で出る電池6種類の反応式・特徴・用途を比較表1枚で完全整理
- 正誤問題で「ひっかけポイント」になる部分をピンポイントで解説
電験三種の機械科目で「電池」が出題されるとき、ほぼ100%が正誤問題です。「次の記述のうち、誤っているものを選べ」という形式で、電解液の種類・放電時の反応・用途を入れ替えた"ひっかけ"が仕込まれます。
つまり、「なんとなく知っている」では点が取れない分野です。逆に言えば、各電池の特徴を正確に整理しておけば確実に得点できる、コスパの良い単元でもあります。
この記事では、電験三種で問われる電池を「イメージ」と「比較表」で整理します。化学式を丸暗記する必要はありません。「なぜそうなるのか」をイメージで掴めば、正誤問題の選択肢を自信を持って切れるようになります。
目次
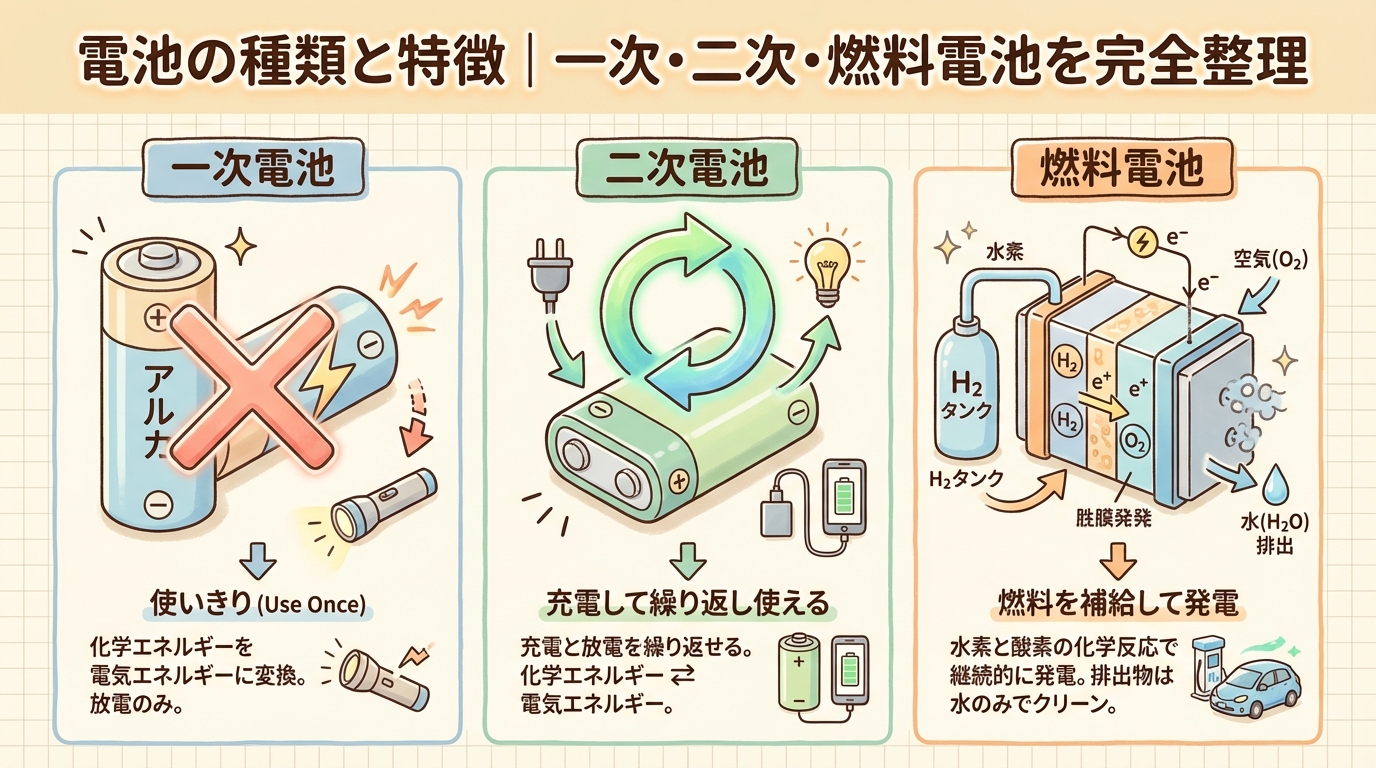
まず全体像|電池は「使い捨て」「充電式」「燃料補給式」の3種類
電池の分類は、実はとてもシンプルです。「使い終わったらどうするか?」で3つに分かれます。
一次電池
使い捨て
化学反応が一方通行。
放電したら終わり。
充電はできない。
例:マンガン乾電池、アルカリ乾電池
二次電池
充電して繰り返し使える
化学反応が可逆(行って戻れる)。
外部から電気を流すと
元の状態に戻る。
例:鉛蓄電池、リチウムイオン電池、NAS電池
燃料電池
燃料を補給し続ける限り発電
水素などの燃料を外部から供給。
電池自体は「発電装置」。
燃料がある限り動き続ける。
例:固体高分子形(PEFC)、リン酸形(PAFC)
「燃料電池は二次電池の一種である」→ これは×(誤り)です。燃料電池は充電して繰り返し使うわけではなく、燃料を外部から供給して発電する装置です。一次電池でも二次電池でもない第3のカテゴリとして覚えてください。
イメージを整理するとこうなります。一次電池は「使い捨てカイロ」、二次電池は「充電式カイロ」、燃料電池は「ガスストーブ」です。ガスストーブはカイロの仲間ではありませんよね。ガス(燃料)を補給して使い続ける「発電装置」です。

一次電池|電験三種での出題頻度は低いが「基本」を押さえる
正直に言うと、一次電池が電験三種で出題されることはほとんどありません。ただし、二次電池・燃料電池との「違い」を正しく理解するための土台になるので、ここで簡単に整理しておきます。
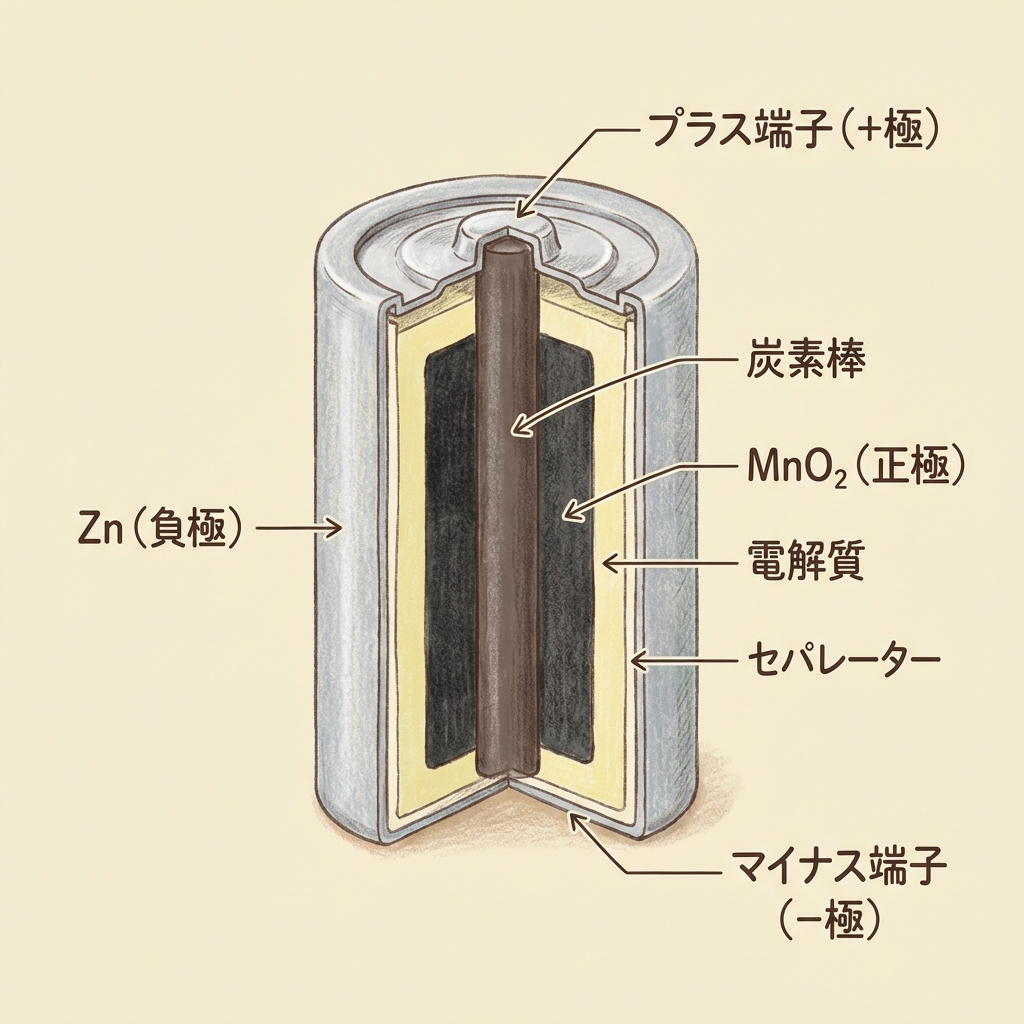
マンガン乾電池とアルカリ乾電池
リモコンや時計に入っている、おなじみの「乾電池」です。どちらも亜鉛(Zn)が負極、二酸化マンガン(MnO₂)が正極という点は同じです。違いは電解液にあります。
| 項目 | マンガン乾電池 | アルカリ乾電池 |
|---|---|---|
| 電解液 | 塩化亜鉛(弱酸性) | 水酸化カリウム(アルカリ性) |
| 起電力 | 約1.5V | 約1.5V |
| 特徴 | 安価。小電流向き (時計、リモコン) |
大容量。大電流OK (ゲーム機、懐中電灯) |
「アルカリ乾電池」の名前の由来は、電解液がアルカリ性(水酸化カリウム)だから。名前がそのまま答えです。電験三種ではここまで深く問われることはまれですが、「一次電池=充電できない」という大前提だけは確実に押さえてください。
二次電池|電験三種の本命。ここが最頻出
電験三種の「電池」問題のほとんどは、この二次電池から出題されます。特に鉛蓄電池・リチウムイオン電池・NAS電池の3つは、それぞれの特徴を混同させる正誤問題が定番です。1つずつ丁寧に見ていきましょう。
① 鉛蓄電池|最も古く、最も出題される「電池の王道」
自動車のバッテリーに使われている、あの重い電池です。1859年に発明された世界初の二次電池であり、150年以上の歴史があります。電験三種でも最も出題頻度が高い電池です。
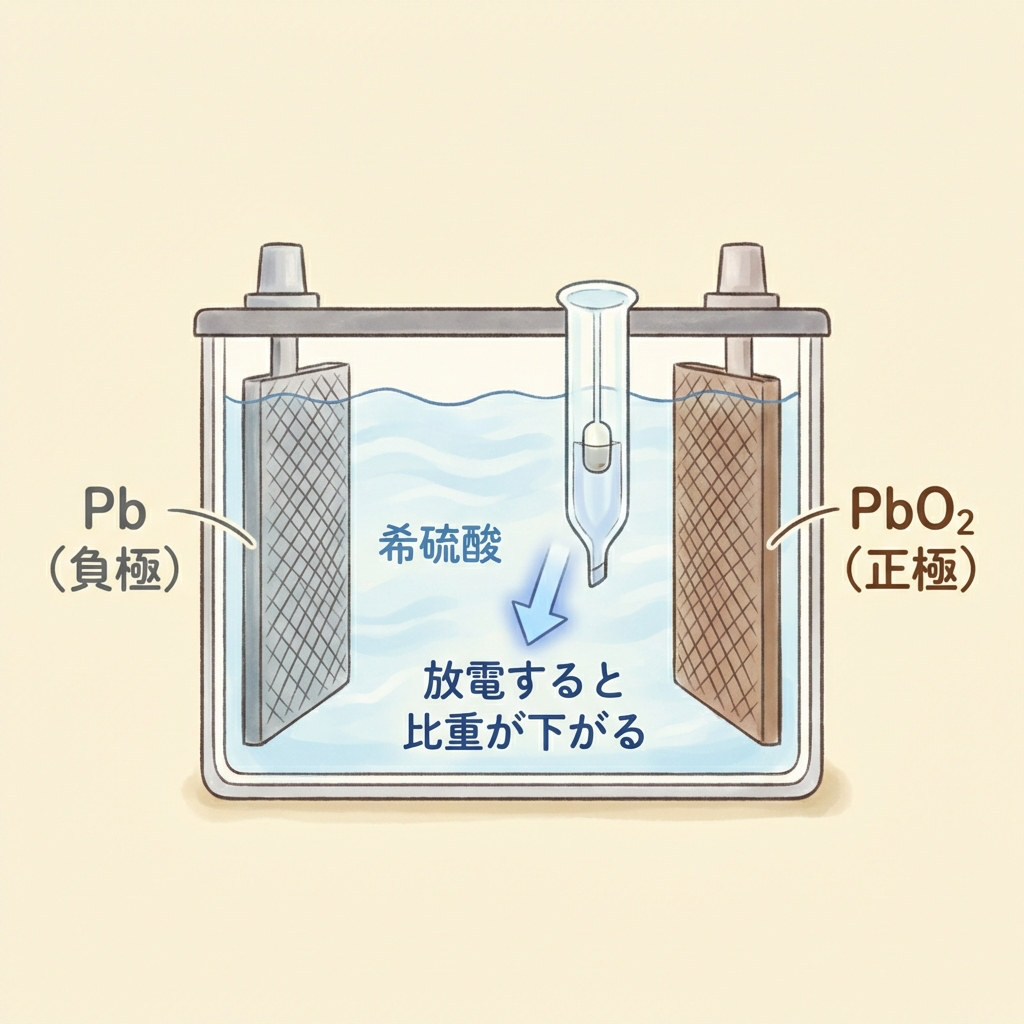
構造をイメージで掴む
鉛蓄電池の構造は、次の3つの要素で成り立っています。
負極(マイナス)
鉛(Pb)
海綿状の鉛の板
電解液
希硫酸(H₂SO₄)
硫酸を水で薄めたもの
正極(プラス)
二酸化鉛(PbO₂)
鉛に酸素がくっついたもの
放電と充電で「何が起きているか」をイメージする
鉛蓄電池の放電反応を、化学式で書くとこうなります。
→(右向き)が放電、←(左向き)が充電
化学式を丸暗記する必要はありません。大事なのは「放電するとどうなるか」のイメージです。
🔍 放電時に起きること(3つのポイント)
① 両極とも硫酸鉛(PbSO₄)に変わる
負極の鉛も、正極の二酸化鉛も、放電すると両方とも硫酸鉛という同じ物質に変わります。「放電すると両極が同じ物質になる」と覚えてください。
② 電解液(希硫酸)が薄くなる
硫酸(H₂SO₄)が極板と反応して消費され、代わりに水(H₂O)ができます。つまり放電すると電解液の比重(濃度)が下がる。
③ 充電すると逆の反応が起きて元に戻る
外部から電気を流すと、硫酸鉛が分解され、鉛と二酸化鉛に戻ります。電解液の濃度も元に戻ります。
「鉛蓄電池は、放電すると電解液の比重が上がる」→ ×(誤り)。放電すると硫酸が消費されるので比重は下がります。これは電験三種で繰り返し出題される最頻出の引っかけです。
鉛蓄電池の特徴まとめ
| 起電力 | 約2.0V(1セル当たり) |
| 電解液 | 希硫酸(H₂SO₄水溶液) |
| メリット | 安価。大電流が取り出せる。技術が成熟している |
| デメリット | 重い(鉛だから)。過放電すると劣化する(サルフェーション) |
| 用途 | 自動車バッテリー、UPS(無停電電源装置)、非常用電源 |
② リチウムイオン電池|スマホからEVまで。現代社会を支える主役
あなたが今このページを読んでいるスマホやPCにも、リチウムイオン電池が入っています。2019年にノーベル化学賞を受賞した吉野彰氏が実用化に貢献したことでも有名です。電験三種では鉛蓄電池との「違い」を問う問題が出ます。
構造をイメージで掴む
負極(マイナス)
炭素(グラファイト)
電解液
有機溶媒
(水は使わない!)
正極(プラス)
リチウム金属酸化物
(LiCoO₂ など)
動作原理のイメージ
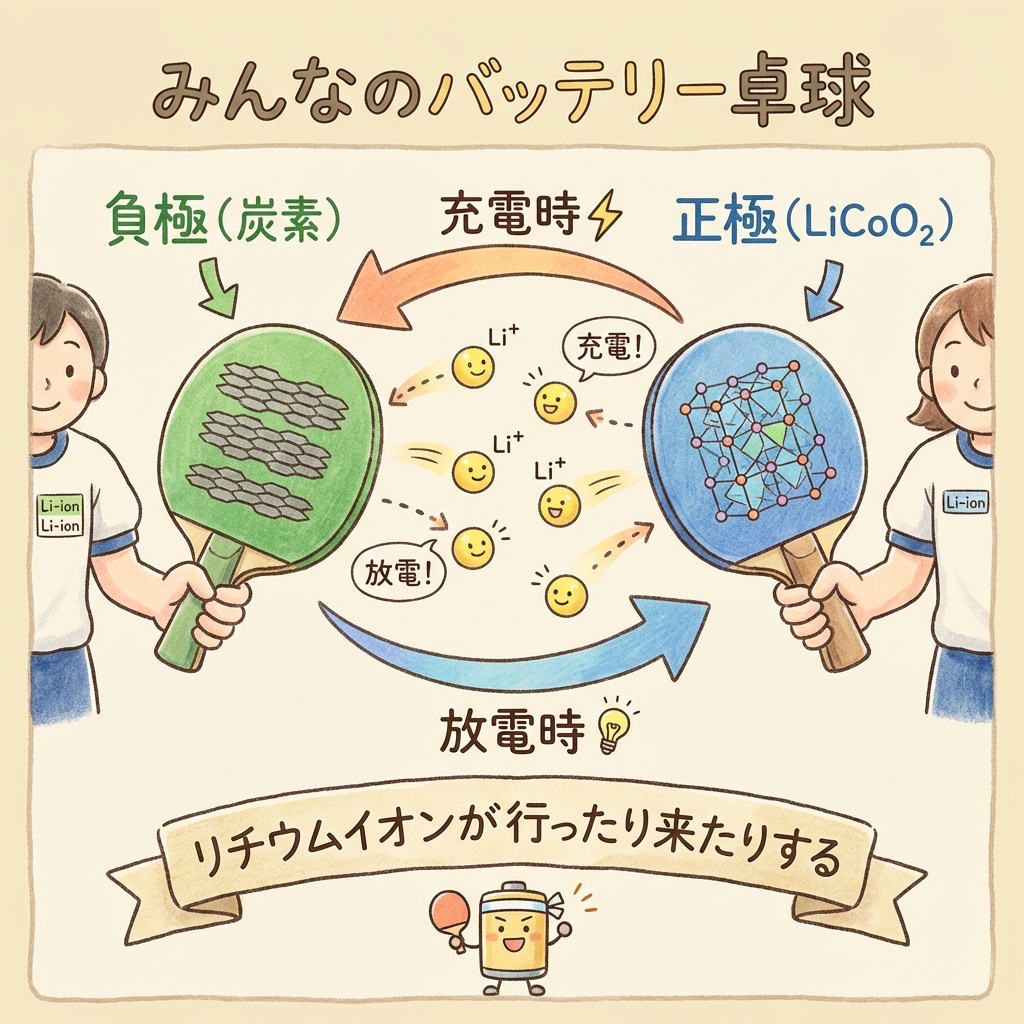
リチウムイオン電池の動作は、鉛蓄電池とは根本的に違います。鉛蓄電池が「極板の材料が化学変化する」のに対し、リチウムイオン電池は「リチウムイオン(Li⁺)が正極と負極の間を行ったり来たりする」だけです。
🏓 卓球で例えると…
リチウムイオン(Li⁺)は「ボール」、正極と負極は「ラケット」です。
放電時:ボール(Li⁺)が負極から正極に飛んでいく。
充電時:ボール(Li⁺)が正極から負極に戻ってくる。
極板自体は大きく変化せず、リチウムイオンが「挿入(インターカレーション)」と呼ばれる仕組みで極板の隙間に出入りします。このため、極板の劣化が少なく、長寿命です。
リチウムイオン電池の特徴まとめ
| 起電力 | 約3.6〜3.7V(1セル当たり)。鉛蓄電池の約1.8倍 |
| 電解液 | 有機溶媒(水を使わない=「非水系」) |
| メリット | 高電圧・軽量・高エネルギー密度。メモリー効果がない |
| デメリット | 過充電・過放電に弱い(保護回路が必要)。高温で発火リスク |
| 用途 | スマホ、ノートPC、EV(電気自動車)、家庭用蓄電池 |
「リチウムイオン電池の電解液は水酸化カリウム水溶液である」→ ×(誤り)。リチウムイオン電池は水を使いません。電解液は有機溶媒(非水系)です。水酸化カリウムはニッケル水素電池の電解液なので、わざと入れ替える問題が出ます。
③ NAS電池(ナトリウム硫黄電池)|電力系統の「巨大蓄電池」
NAS電池は、一般の人にはほとんど知られていませんが、電験三種では頻出の電池です。日本ガイシ(NGK)が世界で唯一量産している、電力貯蔵用の大型蓄電池です。名前の由来は、Na(ナトリウム)とS(硫黄)の頭文字です。
構造をイメージで掴む
負極(マイナス)
ナトリウム(Na)
溶融状態(液体のNa)
電解質
β-アルミナ固体電解質
(液体ではなく固体!)
正極(プラス)
硫黄(S)
溶融状態(液体のS)
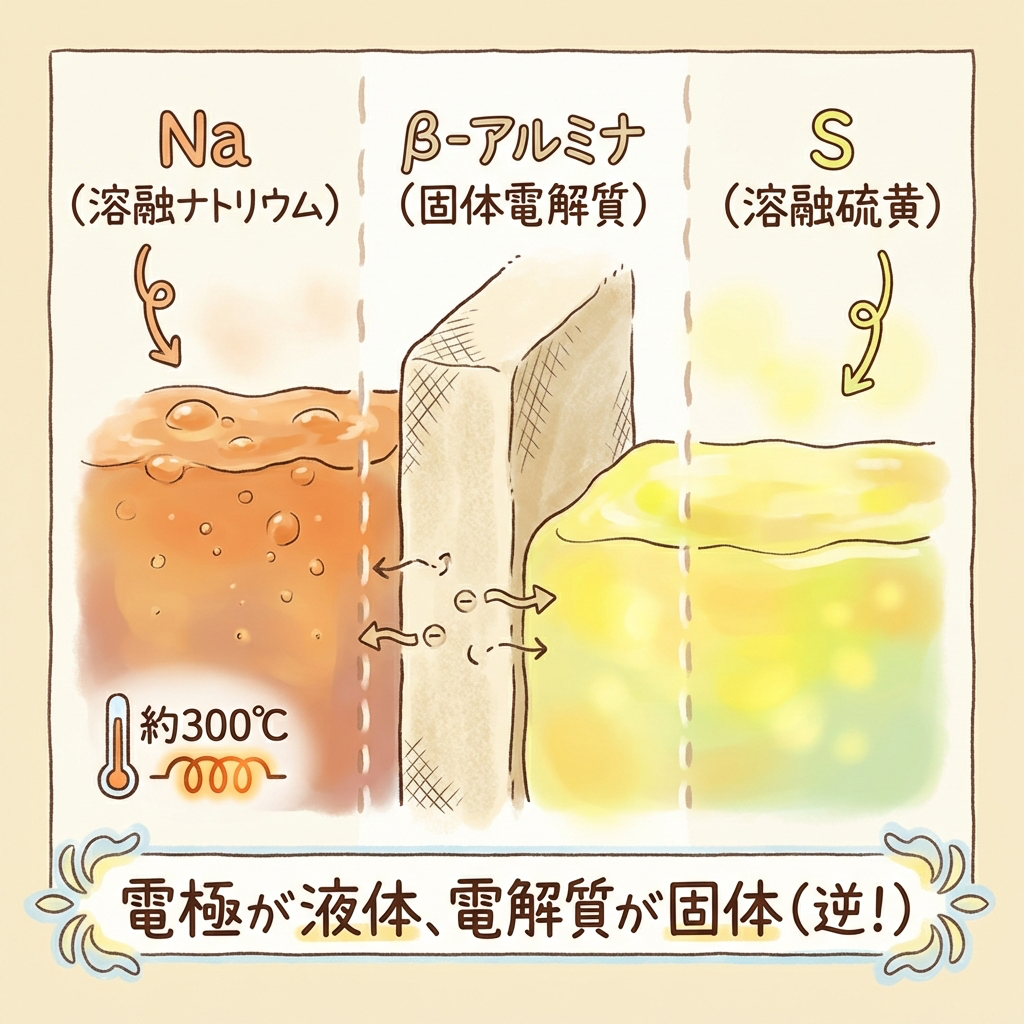
NAS電池の最大の特徴:「高温で動く」
NAS電池の最大の特徴は、約300℃の高温で運転することです。なぜ高温が必要なのか? 理由は単純で、ナトリウムと硫黄を液体(溶融状態)にしておく必要があるからです。
そして、一般的な電池の「液体の電解液」と「固体の電極」という構造が逆になっていることにも注意してください。NAS電池は電極が液体、電解質が固体です。ここは正誤問題で入れ替えて出題されます。
放電するとナトリウムと硫黄が反応して多硫化ナトリウム(Na₂Sₓ)ができる
| 起電力 | 約2.0V(1セル当たり) |
| 運転温度 | 約300℃(高温運転) |
| 電解質 | β-アルミナ固体電解質(液体ではない!) |
| メリット | 大容量・長寿命(約15年)。エネルギー密度が鉛蓄電池の約3倍 |
| デメリット | 高温維持にエネルギーが必要。ナトリウムは水に触れると発火する危険性 |
| 用途 | 電力系統の負荷平準化(夜間に蓄電→昼間に放電)、大規模蓄電設備 |
❌「NAS電池の電解質は液体である」→ ×。固体(β-アルミナ)です。
❌「NAS電池は常温で運転する」→ ×。約300℃の高温で運転します。
❌「NAS電池はスマートフォンに使用される」→ ×。大規模な電力貯蔵用です。
④ ニッケル水素電池|「電解液の入れ替え問題」で登場する脇役
ニッケル水素電池そのものが深く出題されることは多くありませんが、「電解液に水酸化カリウム(KOH)を使う」という特徴が、リチウムイオン電池との入れ替え問題で登場します。ハイブリッド車(プリウスなど)のバッテリーとしても有名です。
| 正極 | 水酸化ニッケル(NiOOH) |
| 負極 | 水素吸蔵合金(MH) |
| 電解液 | 水酸化カリウム水溶液(KOH) ← これが試験で狙われる |
| 起電力 | 約1.2V |
| 用途 | ハイブリッド車、充電式の単三・単四電池(エネループ等) |
・鉛蓄電池 → 希硫酸(酸性)
・ニッケル水素電池 → 水酸化カリウム(アルカリ性)
・リチウムイオン電池 → 有機溶媒(非水系)
・NAS電池 → β-アルミナ固体電解質(固体)
4つとも全部違います。「電解液を入れ替えた選択肢」に引っかからないよう、セットで覚えてください。

燃料電池|「水素と酸素で発電」の仕組みと種類
燃料電池は、一次電池でも二次電池でもない「第3の電池」です。水素(H₂)と酸素(O₂)を外部から供給し続けることで、電気と水(H₂O)を生み出します。
燃料電池の基本原理|「水の電気分解の逆」
中学校の理科で「水に電気を流すと水素と酸素に分解される(水の電気分解)」を習ったことがあると思います。燃料電池は、その逆の反応です。
副産物は「水」だけ。CO₂が出ない = クリーンなエネルギー
・燃料電池は化学エネルギーを直接電気エネルギーに変換する(「燃焼」はしない)
・火力発電のように「化学→熱→運動→電気」という多段階の変換を経ないため、理論的な変換効率が高い(カルノーサイクルの制約を受けない)
・副産物は水だけなので環境にやさしい

燃料電池の種類|電解質で4タイプに分かれる
燃料電池は、使っている電解質の種類によって4タイプに分類されます。電験三種ではこの4種類の「名前・電解質・動作温度・用途」の組み合わせを問う正誤問題が出ます。
| 種類 | 略称 | 電解質 | 動作温度 | 用途・特徴 |
|---|---|---|---|---|
| 固体高分子形 | PEFC | イオン交換膜 (高分子膜) |
約80℃ (低温) |
家庭用(エネファーム)、FCV(燃料電池自動車)。小型・起動が速い |
| リン酸形 | PAFC | リン酸 (H₃PO₄) |
約200℃ (中温) |
業務用・産業用。最も早く商用化された。ビル・病院の分散電源 |
| 溶融炭酸塩形 | MCFC | 溶融炭酸塩 (Li₂CO₃等) |
約650℃ (高温) |
大規模発電所向け。高温のため内部改質が可能。白金触媒が不要 |
| 固体酸化物形 | SOFC | 安定化ジルコニア (固体セラミック) |
約1000℃ (超高温) |
発電効率が最も高い。家庭用エネファーム type S にも採用。白金触媒が不要 |
略称の頭文字で動作温度の「低い順」を覚えましょう。
P → P → M → S(ペペムス)
PEFC(80℃)→ PAFC(200℃)→ MCFC(650℃)→ SOFC(1000℃)
動作温度が上がるほど「大規模発電向け」になり、下がるほど「家庭・車向け」になる、と覚えれば用途も自然に結びつきます。
❌「固体高分子形燃料電池(PEFC)は約1000℃の高温で動作する」→ ×。PEFCは約80℃の低温です。1000℃はSOFCです。
❌「燃料電池はカルノーサイクルの制約を受ける」→ ×。燃料電池は化学エネルギーを直接電気に変換するため、熱機関ではなく、カルノーサイクルの制約を受けません。

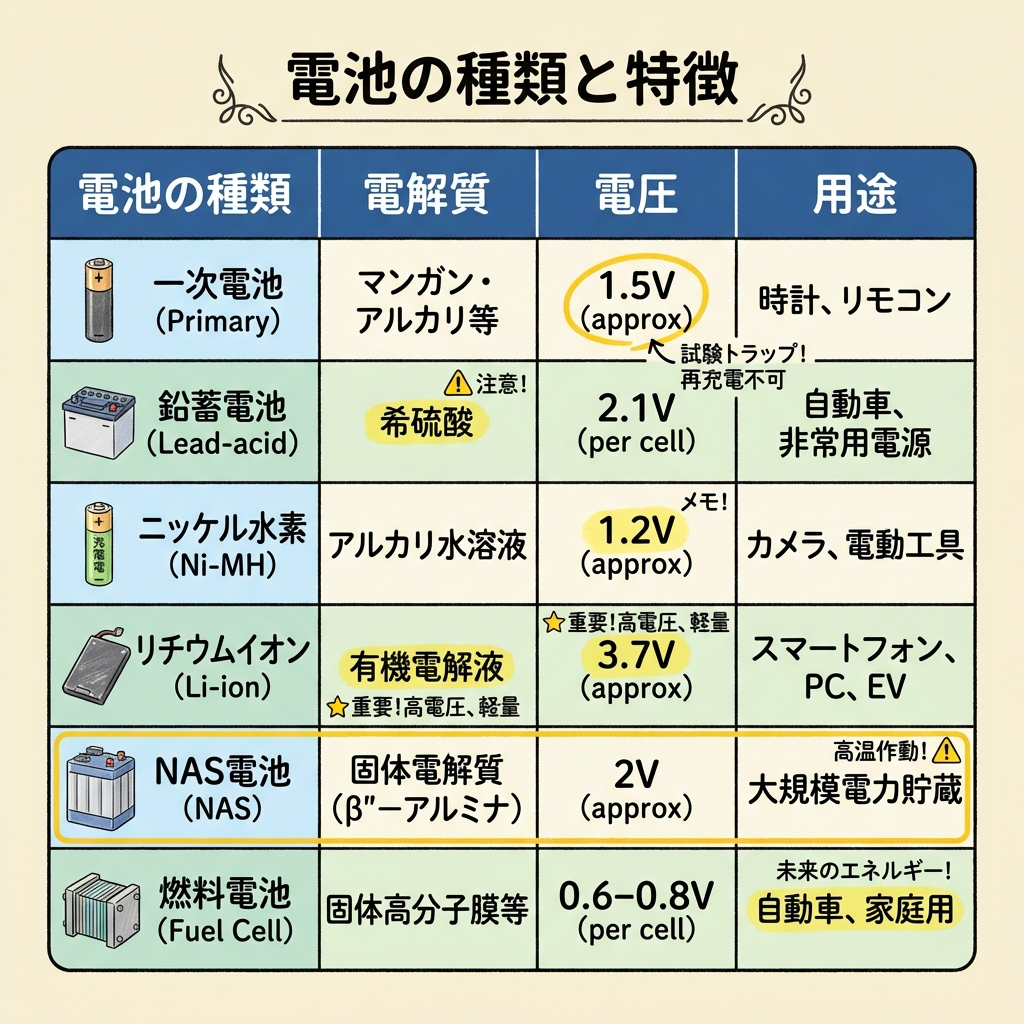
【保存版】全電池の比較表|正誤問題はこの1枚で攻略
ここまでの内容を1枚の比較表に集約します。正誤問題で迷ったら、この表を思い出してください。太字の部分が「入れ替え出題」で狙われるポイントです。
| 分類 | 電池名 | 正極 | 負極 | 電解質 | 起電力 | 特徴・用途 |
|---|---|---|---|---|---|---|
| 一次電池 | マンガン/ アルカリ乾電池 |
MnO₂ | Zn | 塩化亜鉛 /KOH水溶液 |
1.5V | 使い捨て。リモコン・時計 |
| 二次電池 | 鉛蓄電池 | PbO₂ | Pb | 希硫酸 | 2.0V | 安価・大電流。自動車バッテリー、UPS。放電で比重↓ |
| リチウムイオン | LiCoO₂等 | 炭素 (グラファイト) |
有機溶媒 (非水系) |
3.6V | 高電圧・軽量。スマホ、EV。メモリー効果なし | |
| NAS電池 | S(硫黄) | Na | β-アルミナ (固体) |
2.0V | 300℃高温運転。電力系統の負荷平準化。電極が液体 | |
| 燃料電池 | PEFC | 空気極 (O₂) |
燃料極 (H₂) |
高分子膜 | 0.7〜 1.0V |
80℃。家庭用エネファーム、FCV |
| PAFC | リン酸 | 200℃。業務用・ビル電源 | ||||
| MCFC | 溶融炭酸塩 | 650℃。大規模発電。白金不要 | ||||
| SOFC | 安定化ジルコニア | 1000℃。最高効率。白金不要 |
製造現場のUPS(無停電電源装置)に鉛蓄電池が使われていることは多いです。「なんでこんなに重いんだ」と思ったら、中身は鉛の板と希硫酸。構造がわかると、あの重さにも納得できます。最近はリチウムイオン電池に置き換わりつつありますが、コスト面で鉛蓄電池はまだまだ現役です。
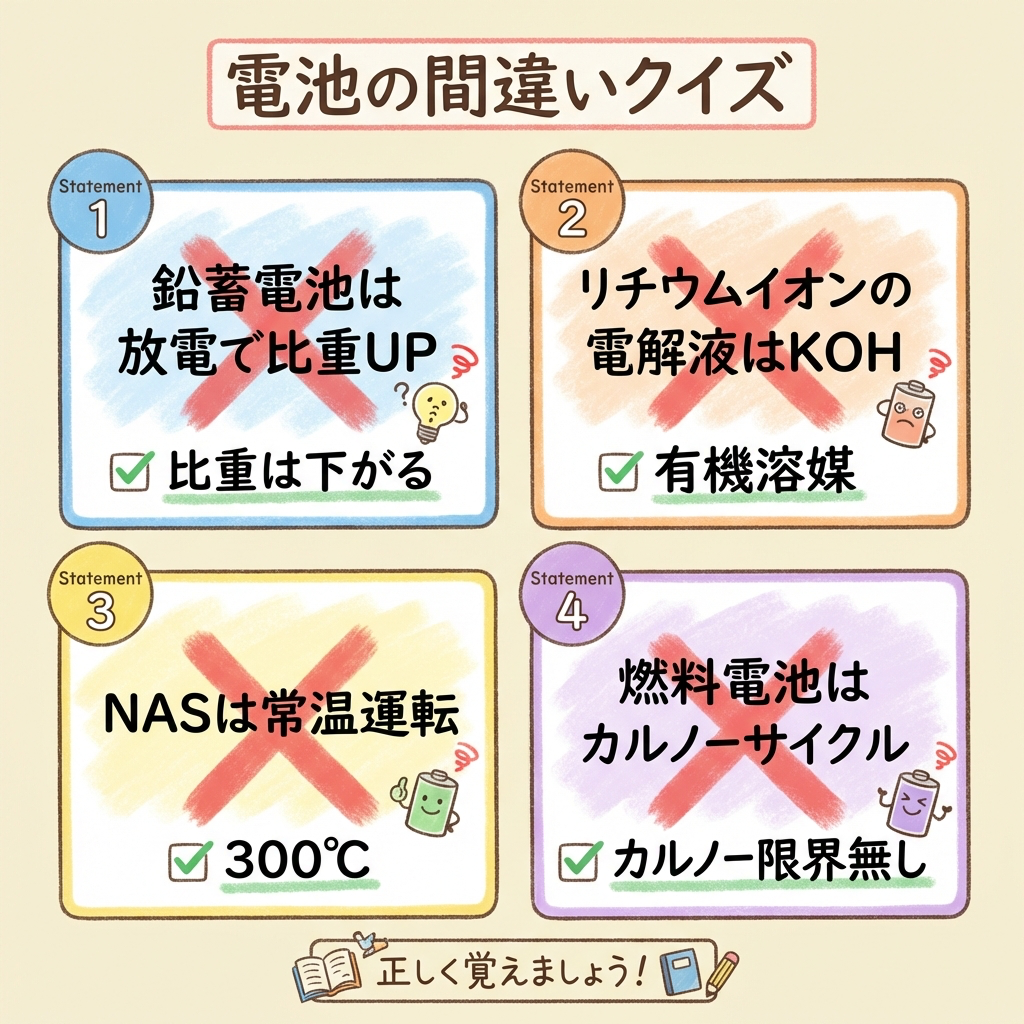
正誤問題で狙われる「ひっかけポイント」総整理
最後に、電験三種の正誤問題で繰り返し出題される「ひっかけパターン」を一覧にまとめます。試験前にここだけ見返せば、確実に1〜2問を拾えます。
| No. | ひっかけ選択肢の例 | 正誤 | 正しい知識 |
|---|---|---|---|
| 1 | 鉛蓄電池は放電すると電解液の比重が上がる | × | 放電で硫酸が消費→比重は下がる |
| 2 | リチウムイオン電池の電解液は水酸化カリウムである | × | 有機溶媒(非水系)。KOHはニッケル水素電池 |
| 3 | NAS電池は常温で運転する | × | 約300℃の高温で運転 |
| 4 | NAS電池の電解質は液体である | × | β-アルミナ固体電解質。電極が液体 |
| 5 | 燃料電池は二次電池の一種である | × | 一次でも二次でもない第3のカテゴリ |
| 6 | 燃料電池はカルノーサイクルの制約を受ける | × | 化学→電気の直接変換。熱機関ではない |
| 7 | 固体高分子形燃料電池(PEFC)は約1000℃で動作する | × | PEFCは約80℃。1000℃はSOFC |
| 8 | リチウムイオン電池にはメモリー効果がある | × | メモリー効果なし。あるのはニッケル水素電池 |
電験三種の電池問題の本質は、「電解質の入れ替え」です。次の3つをセットで暗記してください。
🔴 鉛蓄電池 = 希硫酸(酸性)
🔵 リチウムイオン電池 = 有機溶媒(水を使わない)
🟡 NAS電池 = β-アルミナ固体(液体の電解質ではない)
この3つの組み合わせを「うっかり入れ替えてしまう」のが、不正解の原因No.1です。
まとめ
この記事では、電験三種・機械科目で出題される電池を「一次電池・二次電池・燃料電池」の3分類で整理しました。
📝 この記事のポイント
✅ 電池は「使い捨て(一次)」「充電式(二次)」「燃料補給式(燃料電池)」の3分類
✅ 鉛蓄電池は希硫酸、リチウムイオンは有機溶媒、NASはβ-アルミナ固体──電解質の入れ替え問題が最頻出
✅ 鉛蓄電池は放電で比重が下がる(上がるは×)
✅ NAS電池は約300℃の高温運転。電極が液体で電解質が固体(通常と逆)
✅ 燃料電池は二次電池ではない。カルノーサイクルの制約を受けない
✅ 燃料電池4種類はPEFC→PAFC→MCFC→SOFCの順で温度が上がる
電池の問題は「知っているか知らないか」で決まる知識問題です。計算は出ません。つまり、この記事の比較表を頭に入れておけば、確実に得点できる分野です。試験前にもう一度、比較表とひっかけポイント一覧を見返してみてください。
📚 次に読むべき記事
電池と関連が深い「電気分解」の計算方法。ファラデーの法則を途中式ありで解説します。
機械科目の全分野の出題傾向と、効率的な勉強順序がわかるロードマップ記事です。
合格者が「もっと早く買えばよかった」と後悔したアイテムをランキング形式で紹介。