- 「ファラデーの法則」と聞くだけで化学のトラウマが蘇る
- 公式に出てくる「原子量」「価数」「ファラデー定数」の意味がわからない
- W = AIt / zF は見たことあるけど、何を何で割っているのか理解できていない
- 電気の資格なのに化学が出てくること自体が理不尽に感じる
- 電気分解の仕組みを「お金の両替」に例えて直感的に理解
- 公式 W = AIt / zF の各文字の意味を完全把握
- 「原子量」「価数」「ファラデー定数」を30秒で理解できるたとえ話
- 過去問頻出の計算例2パターンを途中式付きで解説
電験三種は電気の試験なのに、なぜか化学の問題が出ます。それが「電気化学」の分野です。
「電気の資格なのに化学はやめてくれ」——その気持ちはよくわかります。しかし、安心してください。電験三種の電気化学で必要な化学の知識は中学理科レベルで十分です。
しかもこの分野、やることはたった1本の公式に数値を代入するだけです。変圧器やパワエレのような複雑な回路はありません。公式の意味さえ理解すれば、確実に得点できます。
この記事では、化学アレルギーの方でも理解できるように、「お金の両替」という日常の例えを使って、ファラデーの法則を完全攻略します。
目次
電気分解とは?|電気のチカラで物質を「取り出す」技術
電気分解とは、溶液に電流を流すことで化学反応を強制的に起こし、金属などの物質を取り出す技術です。
中学理科で「水の電気分解」をやった記憶はありませんか?水に電流を流すと、水素と酸素に分かれるあの実験です。あれが電気分解です。
・アルミニウムの製錬:ボーキサイトからアルミを取り出す
・銅の電解精錬:純度99.99%の銅を作る
・亜鉛メッキ:鋼板に亜鉛の膜を付ける(自動車のボディなど)
・水の電気分解:水素エネルギーの製造
製造業で働いている方なら、メッキ工程や電解研磨は身近な存在です。
電気分解のイメージ|電気で「鉱石から金属を引っこ抜く」
金属は自然界では「酸化物」や「硫酸塩」として、他の物質とくっついた状態で存在しています。純粋な金属を取り出すには、このくっつきを引き剥がす必要があります。
その「引き剥がす力」が、電気エネルギーです。
(CuSO₄)
(Cu)
電験三種で問われるのは、「どれだけの電流を、どれだけの時間流したら、何グラムの金属が析出するか?」という計算です。これを解くのがファラデーの法則です。

核心|公式の意味を「お金の両替」で理解する
まず、ファラデーの法則の公式を示します。
文字が5つも出てきて「もう無理」と思った方、大丈夫です。この公式はお金の両替と同じ構造です。
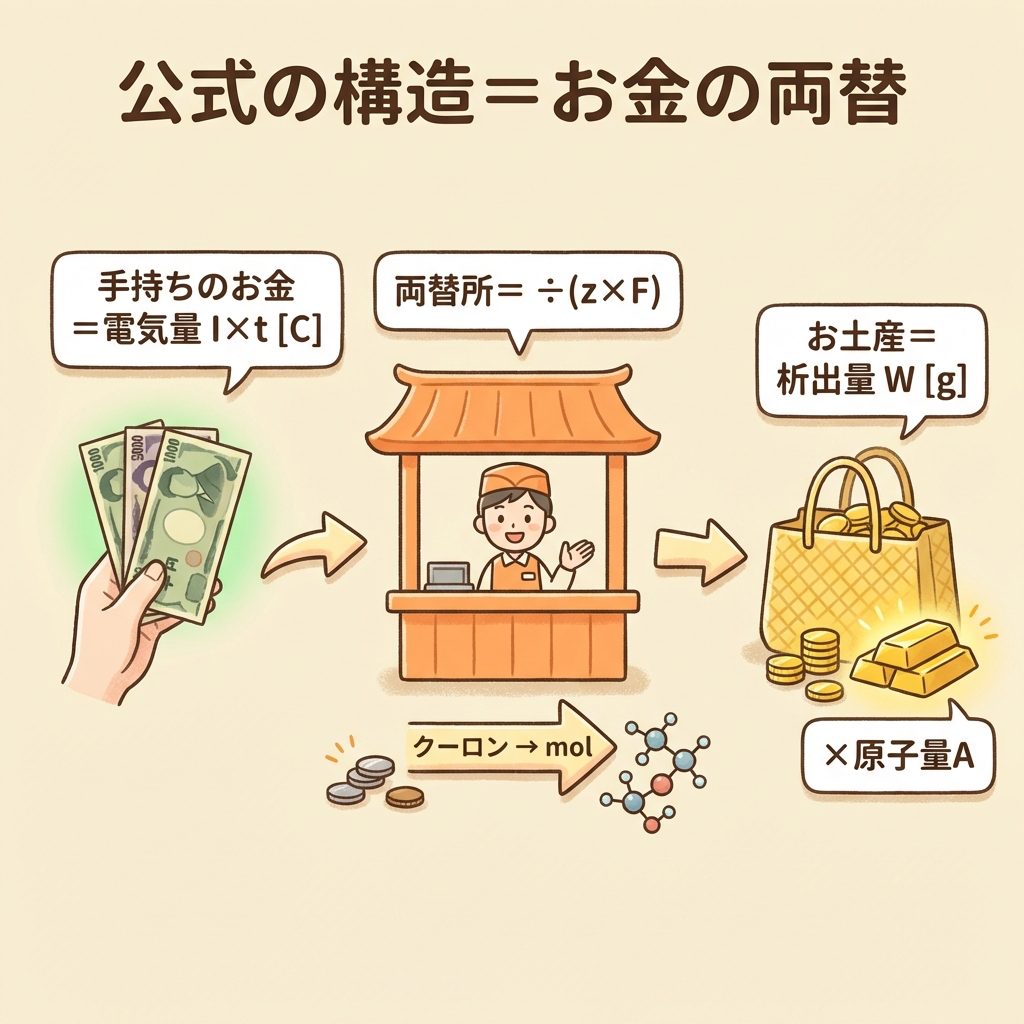
「お金の両替」に例えるとこうなる
海外旅行で「日本円→ドル→現地のお土産」を買う場面を想像してください。
I × t [C]
電子→mol変換
W [g]
つまり、この公式がやっていることは:
② 両替する(電気量 → 金属のmol数に変換する)→ ÷ z × F
③ お土産の重さを計算する(mol → グラムに変換する)→ × A
これだけです。3ステップの「両替計算」をしているだけなのです。
各文字の意味を30秒で理解する
| 記号 | 意味 | 両替のたとえ | 単位 |
|---|---|---|---|
| W | 析出する金属の質量 | 買えたお土産の重さ | [g] |
| A | 原子量(=1molあたりの質量) | お土産1個の重さ | [g/mol] |
| I | 電流 | お金を渡す速さ(1秒あたり) | [A] |
| t | 通電時間 | お金を渡し続ける時間 | [s] |
| z | 価数(=金属1原子が受け取る電子の数) | お土産1個を買うのに必要な硬貨の枚数 | (なし) |
| F | ファラデー定数(= 96,500 C/mol) | 両替レート(電子1mol = 96,500円相当) | [C/mol] |
価数zは問題文で必ず与えられます。「銅の価数は2」「亜鉛の価数は2」「銀の価数は1」のように。覚える必要はありません。
イメージとしては、「金属原子1個を析出させるのに電子が何個必要か」の数字です。銅(Cu²⁺)なら電子2個必要。銀(Ag⁺)なら電子1個でOK。価数が大きいほど、同じ電気量で析出する量は少なくなります。
F = 96,500 C/mol は覚えなくてOKです。電験三種では問題文に「ファラデー定数は96,500 C/molとする」と必ず書いてあります。「約96,500」と頭の片隅に入れておく程度で十分です。
公式 W = AIt / zF の成り立ちを3ステップで追う
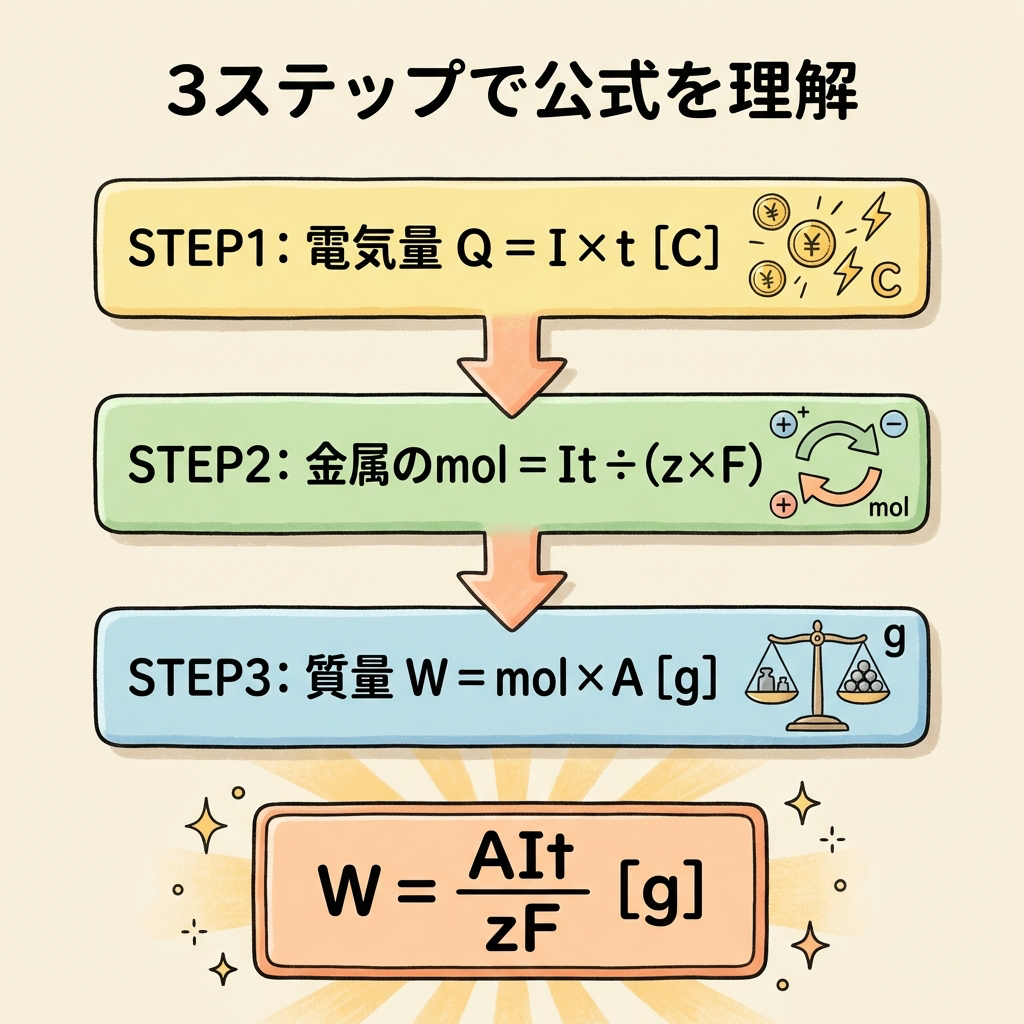
丸暗記ではなく、なぜこの形になるのかを理解しましょう。3ステップで追えます。
STEP 1:電気量を求める(手持ちのお金を数える)
電流I [A] × 時間t [s] = 流れた電気量Q [C]。これは電気の基本ですね。
STEP 2:電気量を「金属のmol数」に両替する
ここが核心です。電気量(クーロン)を金属の量(mol)に変換します。
電子のmol数 = Q ÷ F = It ÷ F [mol]
②次に、金属のmol数を求める(価数zで割る)
金属のmol数 = It ÷ (z × F) [mol]
F(ファラデー定数)= 96,500 C/mol は「電子1mol分の電気量」です。だからQ ÷ Fで「電子が何mol流れたか」がわかります。
さらに、金属1原子を析出させるのに電子がz個必要なので、zで割ると「金属が何mol析出したか」が求まります。
STEP 3:mol数をグラムに変換する(お土産の重さを測る)
W = A × I × t ÷ (z × F) [g]
原子量A [g/mol]は「その金属1molの重さ」です。mol数に原子量を掛ければグラムになります。
Q = I × t [C] (「手持ちのお金」を数える)
mol数 = It ÷ (z × F) [mol] (「両替所」で換金)
W = mol数 × A [g] (「お土産の重さ」を測る)
亜鉛メッキの工程管理では、まさにこの計算で「◯アンペアを◯時間流せば、何μmのメッキ膜が付くか」を見積もります。メッキの膜厚は品質に直結するので、この計算は実務でも使います。
計算例①|亜鉛メッキの析出量を求める
硫酸亜鉛水溶液中で、陰極に2 [A] の電流を5時間通じた。陰極に析出する亜鉛の質量 [g] を求めよ。
ただし、亜鉛の原子量は65.4、価数は2、電流効率は65%、ファラデー定数は96,500 C/mol とする。
STEP 1:情報を整理する
| 電流 I | 2 A |
| 時間 t | 5 h = 5 × 3,600 = 18,000 s |
| 原子量 A | 65.4 g/mol |
| 価数 z | 2 |
| 電流効率 η | 65% = 0.65 |
| F | 96,500 C/mol |
STEP 2:公式に代入する
電流効率がある場合、電気量にηを掛けます(実際に化学反応に使われる電気量はηの分だけ少ない)。
W = 65.4 × 2 × 18,000 × 0.65 ÷ (2 × 96,500)
STEP 3:分子と分母を別々に計算する
= 65.4 × 2 = 130.8
= 130.8 × 18,000 = 2,354,400
= 2,354,400 × 0.65 = 1,530,360
【分母】2 × 96,500 = 193,000
W = 1,530,360 ÷ 193,000
W ≒ 7.93 g
この手の計算は、一気にやろうとすると桁を間違えます。分子を先に計算 → 分母を先に計算 → 最後に割るの3段階が鉄則です。電卓を使える試験なので、落ち着いてやれば必ず正解できます。

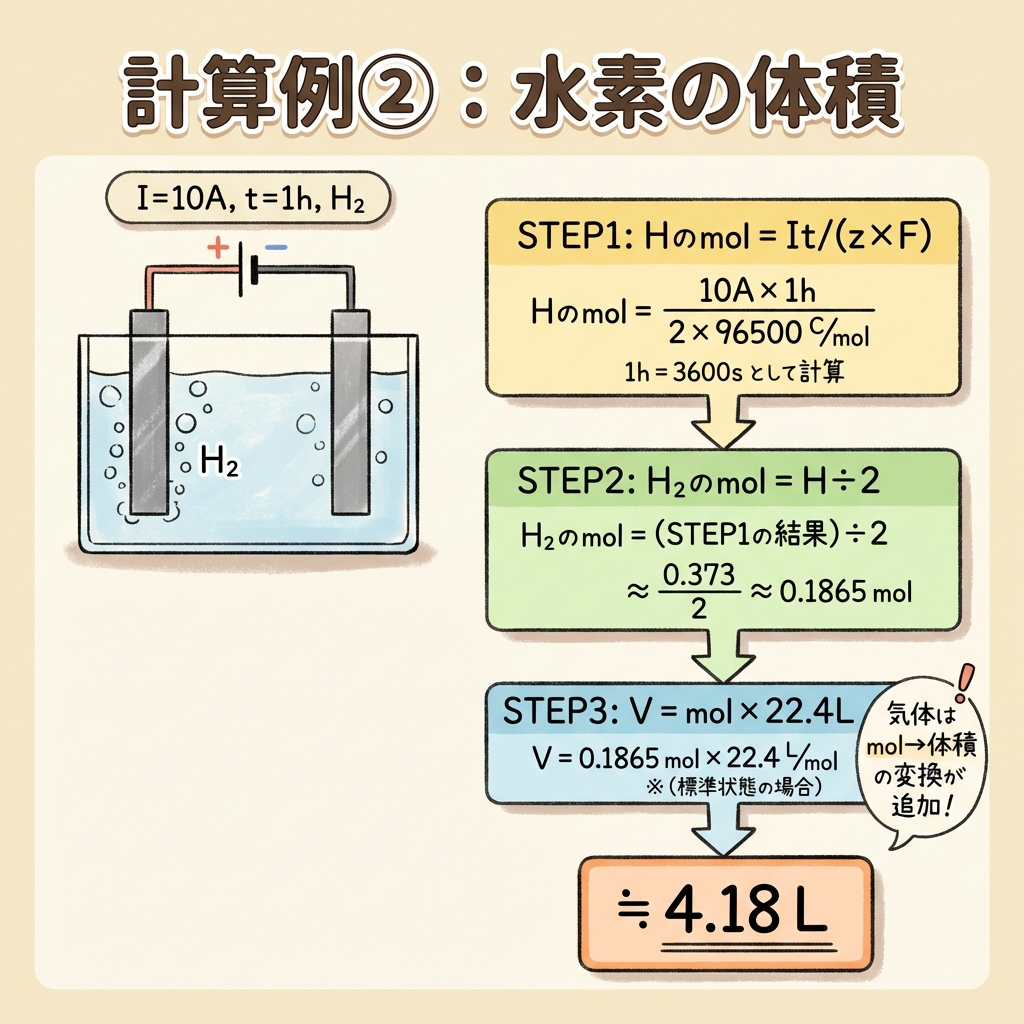
計算例②|水の電気分解で発生する水素の体積を求める
水を電気分解するとき、10 A の電流を1時間流した場合、標準状態で発生する水素の体積 [L] を求めよ。
ただし、水素の原子量は1、価数は1、ファラデー定数は96,500 C/mol、標準状態の気体1 mol の体積は22.4 L、電流効率は100%とする。
STEP 1:情報を整理する
| 電流 I | 10 A |
| 時間 t | 1 h = 3,600 s |
| 水素 H₂ | 分子量 = 2(H原子が2個)、水素イオンH⁺の価数 = 1 |
| 求めるもの | 水素ガス H₂ の体積 [L] |
電気分解で析出するのは水素原子(H)ですが、水素は自然界では分子(H₂)として存在します。つまり、H原子が2個くっついてH₂分子1個になる。このため、最後にH₂のmol数に変換して体積を求める必要があります。
STEP 2:水素原子(H)のmol数を求める
= 10 × 3,600 ÷ (1 × 96,500)
= 36,000 ÷ 96,500
≒ 0.3731 mol(H原子のmol数)
STEP 3:H₂分子のmol数に変換する
= 0.3731 ÷ 2
≒ 0.1866 mol(H₂分子のmol数)
STEP 4:体積に変換する
体積 = 0.1866 × 22.4
≒ 4.18 L
金属の析出量を求める問題ならSTEP 3は「× 原子量 A」でグラムに変換して終わり。しかし気体の場合は「× 22.4 L/mol」で体積に変換します。この違いを意識しておけば、どちらの問題が来ても対応できます。
計算パターンまとめ+ミス防止チェックリスト
出題パターンの整理
| パターン | 求めるもの | 公式の変形 |
|---|---|---|
| A | 析出量 W [g] | W = AIt / zF(基本形) |
| B | 必要な電流 I [A] | I = WzF / At |
| C | 必要な時間 t [s] | t = WzF / AI |
| D | 気体の体積 V [L] | W = AIt/zF で質量 → mol → V = mol × 22.4 |
どのパターンでも、W = AIt / zF を立てて、求めたい変数について解くだけです。
ミス防止チェックリスト
問題文は「5時間」だが、公式のtは秒 [s]。5 × 3,600 = 18,000 s に変換を忘れない。
η = 100%のときは省略できるが、η ≠ 100%のときは電気量にηを掛けるのを忘れがち。
銅:原子量63.5、価数2。亜鉛:原子量65.4、価数2。どちらが分子でどちらが分母か確認。
W [g] で止まらず、mol数 = W/分子量 → 体積 = mol × 22.4 L まで計算する。
W = AIt / zF → 分子にA, I, t、分母にz, F。迷ったら「両替」のステップを思い出す。
W [g] = A [g/mol] × I [A] × t [s] ÷ z × F [C/mol]
単位を追ってみましょう:
[g/mol] × [A] × [s] ÷ [C/mol] = [g/mol] × [C] ÷ [C/mol] = [g] ✅
単位の辻褄が合うかチェックすれば、公式を丸暗記する必要はありません。
まとめ|電気化学は「1本の公式」で得点できる
この記事の内容を振り返ります。
| 1 | 電気分解は「電気の力で金属を取り出す」技術 |
| 2 | 公式はW = AIt / zF の1本だけ |
| 3 | 公式の構造は「お金の両替」と同じ(電気量→mol→グラム) |
| 4 | 原子量A・価数z・ファラデー定数Fはすべて問題文で与えられる |
| 5 | 電流効率ηがあれば電気量にηを掛ける |
| 6 | 気体の問題は追加でmol → 体積(× 22.4 L)の変換 |
| 7 | 最大のミスは時間の単位変換忘れ(時間→秒) |
「電気の資格なのに化学はやめてくれ」と思っていた方も、ここまで読めば気づいたはずです。電験三種の電気化学は、化学の知識はほぼ不要です。
必要なのは「公式に数値を正確に代入する力」と「単位変換を間違えない注意力」だけ。つまり、中学数学レベルの四則演算で解ける分野です。
電熱のQ = mcΔTと合わせて、ファラデーの法則W = AIt/zFもマスターすれば、機械科目の電熱・電気化学分野は盤石です。
電験三種の勉強が加速する!おすすめ便利グッズ・アプリ →
📚 次に読むべき記事
電気化学と同じ「電熱」分野の6種類の加熱方式と熱量計算を整理できます。
機械科目全体の攻略順序がわかります。電熱・電気化学は最初に固めるべき分野です。
機械科目にどのくらい時間を配分すべきかがわかります。